|
|
IP-MS — 蛋白互相作用研究中的“检测器3034
蛋白-蛋白相互作用(Protein-Protein Interaction, PPI)介导了许多的生物学过程,其在催化、转运、信号传导等许多生命过程中具有重要的意义。鉴定蛋白质与蛋白质之间的相互作用(protein-protein interaction,PPI)是后基因组时代的重要研究内容。
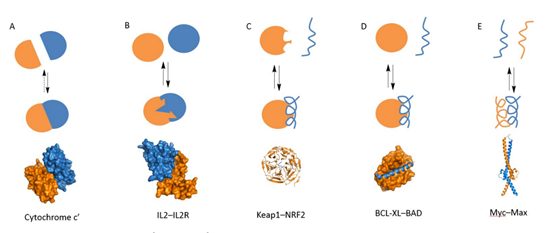
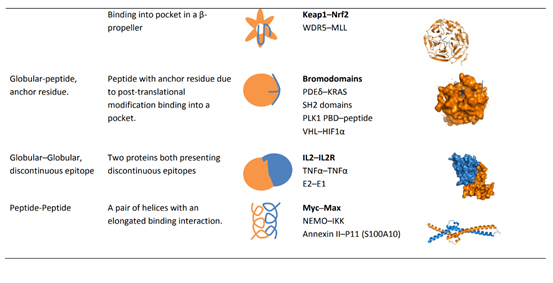
蛋白-蛋白相互作用类型
a:两个球状蛋白预先形成一个表面,然后靠近再产生相互作用 b:两个球状蛋白在靠近过程中,互相诱导产生表面并产生相互作用 c:一种刚性球状蛋白与多肽产生相互作用 d:一种柔性球状蛋白与多肽产生相互作用 e:两个多肽之间产生相互作用
质谱是蛋白互相作用研究中的蛋白质“检测器”
一般的质谱技术是不能直接研究蛋白互相作用的,需要和其他技术联用,比如常见的有免疫共沉淀(CO-IP)和pull down等实验,然后再用质谱这种蛋白质“检测器”来告诉我们样品中存在哪些蛋白,甚至于可以比较不同样本中,这些蛋白的相对丰度,寻找差异蛋白。质谱这种蛋白质检测器与传统的看分子量的SDS-PAGE以及依靠特异性抗体的Western blot(蛋白质印迹法)相比,它不仅能够验证已知蛋白相互作用,还可以鉴定与目标蛋白发生相互作用的未知蛋白。所以它的结果还是很有价值的,这也是大家越来越重视它的原因。
免疫沉淀串联质谱分析(IP-MS)是目前应用最广泛的蛋白相互作用研究方法的一种。IP-MS的主要原理是基于特异性抗体或其他亲和试剂与靶标蛋白的亲和作用,通过免疫共沉淀(co-Immunoprecipitation)将靶标蛋白与靶标蛋白的相互作用蛋白从复杂的样本中提取出来,进而进行质谱检测以鉴定靶标蛋白的相互作用蛋白。 理想的IP-MS实验会通过特异性靶向目的蛋白以检测更接近生理状态下的蛋白相互作用,但这种检测准确性很大程度上会受到目的蛋白内源表达水平低或抗体效价低等因素干扰。因此,过表达目的蛋白并带有融合标签(例如Flag、HA、Myc等)是一种很好的选择。
由于IP-MS实操作上与常用的IP-WB的实验非常相似,但是具体流程需要随质谱仪器性能的提升和数据分析方法的发展对实验方法和策略进行调整和优化。
Biolinkedin将分享以下一些IP-MS建议。
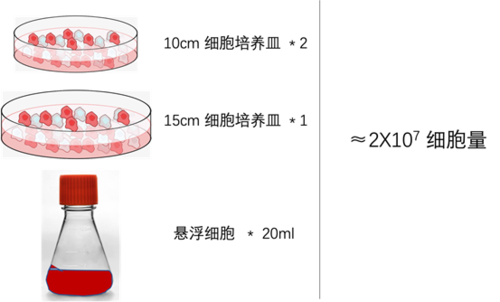
一、细胞用量 IP-MS实验起始细胞用量主要需根据细胞种类、靶标蛋白表达丰度、亲和抗体效价等因素进行调整。通常每个样品起始细胞量建议不少于2x107。如果是靶标蛋白高表达的细胞系,如过表达的标签蛋白,或是细胞内高表达的内源性蛋白(如Actin、RPS等)可适当降低细胞用量,但建议不少于1x107。在一定范围内,细胞用量越多,能够获得的质谱检测结果越好。
二、抗体选择 抗体是决定IP实验是否成功的最关键因素。 有研究统计过数千种商业化抗体的检测效果,其中能够在WB实验中获得良好结果的不到30%,在WB实验中明确结果无效的接近50%。通常来说,IP实验对抗体的要求较WB更高,而为了尽量降低由抗体非特异性导致的假阳性互作鉴定结果,IP-MS中所用的抗体相比传统IP-WB,也会有更高的要求。 因此,用于IP-MS实验的抗体,建议经过以下4步进行筛选和验证:
(1)尽量选择已标明可用于IP实验的抗体,尤其是已发表高分文献中引用的品牌以及货号。 (2)查询抗体生产厂商及以前使用者提供的使用结果。 (3)购买抗体后进行IP-WB预实验,根据结果判断抗体效果。优先选择条带大小与靶标蛋白一致,且无其他非特异性条带的抗体。 三、Beads
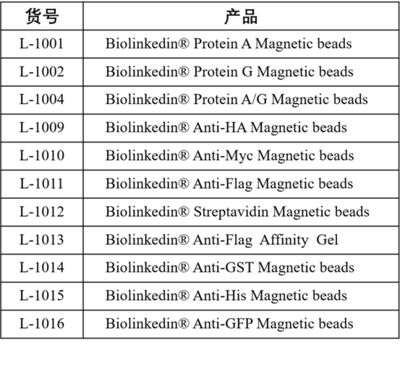
目前常用的基质材料有两种,一种是琼脂糖凝胶(Agarose/Sepharose),另一种是磁珠(Magnetic beads)。相比琼脂糖凝胶,磁珠通常亲和效价更高,操作更简单,清洗效果更好,但成本也稍高。在IP-MS实验中更建议使用磁珠进行实验。 Beads中的IgG结合蛋白通常可分为Protein A,Protein G和Protein A/G。针对IP实验中最常用的鼠抗和兔抗,Protein A和Protein G均能有效结合,但二者针对其他种属的抗体结合能力略有差异。Protein A/G是同时含有Protein A和Protein G抗体结合结构域的融合蛋白,对绝大部分IP实验中采用的抗体均能有效结合。 当然,如果是过表达外源性靶蛋白并带有融合标签(例如Flag、HA、Myc等) 可以直接使用标签抗体磁珠,如Biolinkedin®Anti-Flag Magnetic beads ,省去磁珠与抗体偶联这一步,更加便捷。 PS: Biolinkedin免疫沉淀系列
四、裂解液、清洗液和洗脱液
裂解液通常主要由去垢剂、抑制剂和缓冲体系三部分组成。
IP所用的裂解液中,去垢剂通常为 0.5%-2%的NP40或TritonX-100,也可二者联合使用。为了提高裂解效率,少数裂解液中也会含有0.01%浓度的SDS或SDC。但需要注意的是,其他裂解液中常用的高浓度SDS(>0.1%)会破坏蛋白与蛋白的相互作用,因此通常不能使用在IP实验中。
由于IP实验需要进行孵育,为了避免蛋白降解,裂解液中通常需要加入蛋白酶抑制剂。此外也可根据靶标蛋白类型及具体的研究目的,额外添加磷酸酶抑制剂等。
IP缓冲液中常见的缓冲体系为150 mM NaCl/50 mM Tris-HCl,pH 7.5。不同课题组和研究者所用的盐浓度和pH值可能略有差异。需要注意的是,高盐浓度的缓冲体系(>300 mM NaCl)会很大程度上破坏较弱的蛋白相互作用,导致质谱检测的蛋白鉴定结果急剧减少。
在常规的IP-WB实验中,通常可直接以裂解液作为清洗液,以含有高浓度SDS、溴酚蓝和β-巯基乙醇的loading buffer作为洗脱液。但在IP-MS实验中,为了更适配后续的质谱检测样品处理,需要清洗之后的样品中不含有去垢剂成分。因此建议以不含去垢剂的缓冲体系,或在常规清洗液清洗后,以PBS或缓冲体系进行清洗置换。为了尽量保留样品中的互作蛋白,避免样品制备过程中的蛋白损失,建议清洗之后直接以beads沉淀进行后续用于质谱检测的样品制备,而不进行蛋白的洗脱。
五、设置对照组以及重复实验
设置对照组的目的就是通过对比对照组结果,能更好的剔除假阳性结果。同时,为了避免单次实验的偶然误差,尽可能增重复实验次数,虽然这样前期研究成本会上升,但是对于筛选出高可信度的相互作用蛋白尤为重要,并且会大大降低后期蛋白相互作用验证的工作量。所以整体来看,增加了结果可靠性,其实成本反而是下降的。
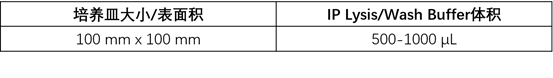
Biolinkedin提示具体实验步骤可参考 操作流程 贴壁细胞样品: 1. 移去培养基,用 PBS 洗细胞两次。 2. 收集细胞至1.5 mL EP 管内,按比例加入Biolinkedin®IP Lysis/Wash Buffer,同时加入PMSF等相应的抑制剂,混匀后置于冰上静置5-20min(期间混匀几次)。 3. 4 ℃,12000-16000 g,10 min离心收集上清液,置于冰上以备后续实验(或置于-80 ℃长期保存)。 培养皿IP Lysis/WashBuffer推荐使用体积:
悬浮细胞样品: 1. 4℃、500-1000 g、10 min,收集细胞,弃上清。 2. 用PBS 洗细胞一次,即用 PBS 将细胞团重悬,4℃、500-1000 g、10 min,收集细胞,弃上清。 3. 用预冷的IP Lysis/Wash Buffer重悬细胞。同时加入PMSF等相应的抑制剂,混匀后冰上静置5-20 min(期间混匀几次)。 4. 4 ℃, 12000-16000 g,10 min离心收集上清液,置于冰上以备后续实验(或置于-80 ℃长期保存)。 免疫复合物的制备 注意:样品所需的量和孵育时间均依赖于每个特定的抗体-抗原体系,因而可能需要优化才能得到最大产量。 以下实验方案针对5-15μg 亲和纯化的抗体,根据需要可以按比例放大。 1. 在离心管中,将每个样品的细胞裂解液与免疫沉淀抗体结合。 2. 用IP Lysis/Wash Buffer将抗体以及制备好的样品稀释至500μL-800μL。 3. 在4 ℃ 孵育2-4h或者过夜,以形成免疫复合物。 免疫沉淀: 注意:为保证磁珠均匀分布,使用前通过反复颠倒或轻微涡旋混匀瓶中磁珠。 1. 将50-200µL的Biolinkedin® Protein A/G Magnetic Beads加入1.5 mL 离心管中。 2. 向磁珠中加入500 -1000µL 预冷PBS,轻柔混匀。 3. 将离心管放入磁力架中收集磁珠到离心管的一边。去除上清。 4. 向离心管中加入500-1000 µL IP Lysis/Wash Buffer。颠倒离心管数次或轻微涡旋混匀1min。用磁力架收集磁珠。去除上清。 5. 将抗原样品/抗体混合物加入装有磁珠的离心管中,保持混匀4 ℃ 孵育4-6h或者过夜。 6. 用磁力架收集磁珠,除去未结合的样品,保存以备分析。 7. 向离心管中加入800 -1000 µLIP Lysis/WashBuffer,轻柔混匀数次。收集磁珠,弃上清。再重复洗两次。
质谱送样准备: (一)溶液蛋白定性:(接步骤7) 8. 将蛋白从磁珠上洗脱下来。 9. 最好测定蛋白浓度后,干冰寄送液氮速冻的蛋白溶液(需指明缓冲液成分和浓度);或将蛋白通过TCA法或丙酮法沉淀,晾干后,干冰或冰袋寄送。 a) 缓冲液不含去污剂NP40、Triton X-100等 b) 不含有SDS等物质 c) 推荐使用竞争性洗脱(例如flag标签蛋白被flag多肽竞争洗脱) (二)胶条鉴定样品要求: (接步骤7) 8、向离心管中加入80-100 µL Biolinkedin®SDS-PAGE Sample Loading Buffer(1 ×),将样品置于100℃水浴或者金属浴中加热10 min。通过磁力架分离磁珠,保留含有目的抗原的上清。 9、电泳后通过考马斯亮蓝染色,将蛋白条带用干净的刀片切下,并切割为1 mm3的小块,装入进口EP管中及时送样,送样时需加冰袋维持低温。 样品要求 a) 蛋白质溶液:浓度>0.1μg/μl,蛋白质总量 >5μg; b) 缓冲液不含去污剂NP40、Triton X-100等 c) SDS-PAGE条带:考染、银染(质谱兼容)条带清晰可见; PS:Biolinkedin系列IP试剂盒均标配抑制剂、裂解液、洗脱液、磁力架 以Biolinkedin® Classic IP/Co-IP Kit (IK-1004)为例 试剂盒组成:
六、结果分析 一般在IP-MS实验中,我们会通过蛋白成分鉴定的方式筛选互作蛋白。通过对比实验组和对照组结果将实验组中蛋白筛选为靶标蛋白的互作蛋白。
不过随着质谱检测灵敏度的不断提升,现在极微量的非特异性结合或清洗残留的背景蛋白也会被检测到,导致检测结果信息量急剧增加;而且很多蛋白之间的相互作用是较弱的、瞬时的、动态的结合,简单的通过蛋白成分鉴定的方式未必能全部检测出来。 因此在目前的IP-MS数据分析中,主要以蛋白的非标记定量信号强度(LFQ intensity)作为蛋白定量数据,比较实验组与对照组间蛋白定量差异,与常规定量蛋白质组学数据分析方法类似,只是通常选择更高的差异蛋白筛选阈值。 因此,在目前的IP-MS实验中,通常会选择较为温和的清洗条件,以保留更多的弱相互作用蛋白以及无法避免的背景蛋白和非特异性结合蛋白,之后基于定量蛋白质组学数据,即质谱检测获得的蛋白定量矩阵,通过实验组与对照组的蛋白定量比较筛选高可信的蛋白相互作用,过滤背景蛋白和非特异性结合。 IP-MS结果中Fold Change和Intensity两项指标很关键。Fold Change表示IP实验组和对照组间蛋白的定量差异倍数,Intensity表示IP样品中蛋白的检测信号,可反映样品中的蛋白丰度。通常选择Fold Change和实验组样品中Intensity数值较大,排名靠前的蛋白作为后续研究的重点研究蛋白。 但是我们也要注意,结果中蛋白的Fold Change和Intensity通常低于靶蛋白的Fold Change和Intensity。如果结果明显高于靶蛋白的数值,需要考虑是非特异性结合。 在后期分析中、更需要结合Pubmed、UniProt、STRING等数据来进行全面分析,比如核糖体蛋白(RPS蛋白家族)、细胞骨架蛋白(Actin等),一般需要被忽略。
蛋白质互作网络(PPI, Protein-Protein Interaction Networks)是由蛋白通过彼此之间的相互作用构成,来参与生物信号传递、基因表达调节、能量和物质代谢及细胞周期调控等生命过程的各个环节。系统分析大量蛋白在生物系统中的相互作用关系,对了解生物系统中蛋白质的工作原理,了解疾病等特殊生理状态下生物信号和能量物质代谢的反应机制,以及了解蛋白之间的功能联系都有重要意义,常常与筛选关键基因相关联。
目前常用的制作PPI的工具为STRING数据库(https://cn.string-db.org)。STRING数据库是一个搜索已知蛋白质之间和预测蛋白质之间相互作用的数据库,该数据库可应用于2031个物种,包含960万种蛋白和1380万中蛋白质之间的相互作用。它除了包含有实验数据、从PubMed摘要中文本挖掘的结果和综合其他数据库数据外,还有利用生物信息学的方法预测的结果。
以下为PPI输出图形的结果解读:
网络图(以输入蛋白为中心)
1.节点(node)
图中每个节点表示一个蛋白,由同一个基因产生的不同isoform将被合并,在节点上标记的字母为对应基因的gene symbol。
图中有些节点内部有螺旋状的结构,这表示该蛋白的三维结构已知,如果未知的话,节点内部为空。
默认情况下节点的颜色分成红色和白色,红色代表是你的查询蛋白,白色代表与查询蛋白具有相互作用关系的其他蛋白。由于白色不太好看,string会根据与相互作用的score值对颜色进行映射。Score值详情见下图:
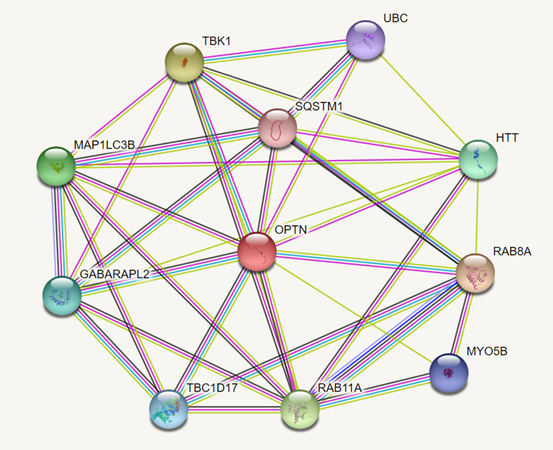
2.边(edge)
节点之间的连线表示两个蛋白之间的相互作用,不同颜色对应不同的相互作用类型,示意如下:
从图中可以看到,两个蛋白之间的连线不止一条,这表示两个蛋白间存在多种相互作用关系。所有的相互关系中,既有实验验证的,也有数据预测的结果。
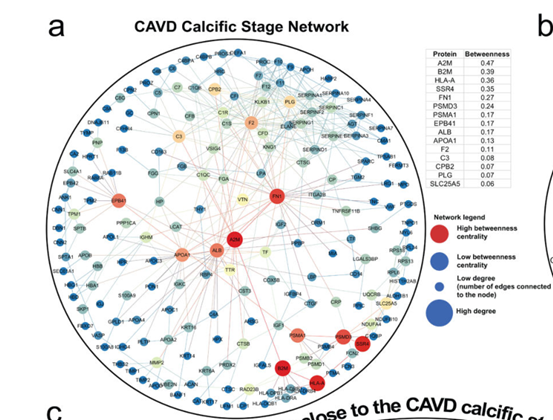
圈图
除了STRING数据库的输出结果,还可以通过Cytoscape等工具加工、美化PPI,其中的一种形式就为圈图,在圆圈上的每个节点都代表一个蛋白,彼此之间的连线则指示彼此之间的相互作用。有 节点的颜色有时指示介数中心度,在本图中,具有高介数中心度的节点被标记为红色,意味着这些蛋白在这个网络中具有中心地位。 另外,蛋白质修饰位点也可以通过质谱方式加以分析确定。 翻译后修饰(Post-translational modifications, PTM)目前规模化研究的蛋白修饰主要有磷酸化(Phosphorylation)、乙酰化(Acetylation)、甲基化(Methylation)、糖基化(Glycosylation)、泛素化(Ubiquitination)等。PTM增加了蛋白质组的复杂性,对蛋白质结构,分布和功能产生巨大影响。它在细胞生物学中起重要作用,包括细胞信号传导,细胞结构,DNA修饰等。同一蛋白在不同生理状态、不同亚细胞定位、不同氨基酸位点的修饰,可能对应不同的功能。因此蛋白质翻译后修饰是当前的一个研究热点和难点。
质谱是一种强大的技术,可用于蛋白质修饰位点的分析。利用质谱技术可以对单一蛋白的修饰位点进行鉴定,也可以进行高通量蛋白质组修饰谱分析。
质谱技术主要是通过测定样品的质荷比(m/z)进行分析。蛋白质经过修饰后,分子量会增加。这种分子量的增加在蛋白质图谱中表现为质谱峰发生相应的漂移。例如,肽段磷酸化后,会产生+80Da的质量偏移。质谱通过检测多肽离子的质量来鉴定肽,从而可以检测出PTM导致的质量偏移,进而识别发生翻译后修饰的蛋白。 七、注意事项 PVDF或者NC膜上的蛋白不能进行质谱检测。 样本准备Q&A: Q:用于质谱检测的蛋白溶液样品溶剂要求? A:蛋白溶液 SDS 含量低于 0.1 % Q:用于质谱检测的蛋白溶液样品蛋白量要求? A:单一蛋白溶液蛋白总量不少于 1 5μg;混合蛋白溶液蛋白总量不少于 50μg(若各成分蛋白含量相差较大,含量较少的蛋白不易被检测到) Q:用于质谱检测的胶条样品大小要求? A:胶条以 1 cm*1 cm 为宜,胶条过大容易导致酶解效率低,建议分成多份进行酶解。 Q:用于质谱检测的胶条样品染色要求? A:胶条一般进行银染或者考染;若检测全部整个泳道蛋白的,可直接固定无需染色;染色无需颜色过深(脱色反而费时) Q:用于质谱检测的胶条样品切胶要求? A:若检测单一蛋白条带,则只切取该蛋白条带位置即可;若检测多个蛋白条带,则分别切取后合并;若检测整个泳道蛋白,建议样品只跑较短时间浓缩胶或分离胶即可切取检测。 Q:用于质谱检测的胶条样品蛋白量要求? A:若为单一蛋白条带,该蛋白量不少于 20μg;若为多个蛋白条带,各个蛋白的蛋白量不少于 20μg;若为整个泳道蛋白,蛋白总量不少于 50μg(其中含量较低的蛋白不易检测);若为纯化后蛋白的互作蛋白条带,建议纯化前蛋白量不少于 5mg(纯化前蛋白量过低,导致纯化后互作蛋白含量较低,检测蛋白数目较少);胶条蛋白量不能依靠胶条染色的颜色深浅来判断,因为显色时间越长,颜色会越深。 Q:纯化后蛋白可以直接使用蛋白溶液进行检测吗? A:不可以,纯化蛋白时通常会使用抗体(亲和纯化不需要),如果不进行 SDS-PAGE 分离,抗体会发生干扰;如果进行兴趣蛋白的互作蛋白的研究,则必须进行SDS-PAGE从而实现将兴趣蛋白排除(。兴趣蛋白一般会是高丰度的表达,不排除会造成检测干扰) Q:蛋白胶点鉴定时,2-DE采用银染染色的方法,是否会对后续的质谱鉴定产生影响? 银染试剂里不要使用戊二醛,因为它会对蛋白进行修饰,这样会影响后续的蛋白鉴定。 Q:胶条鉴定的结果中有很多蛋白,怎么确定这些蛋白的含量高低? 胶条鉴定是一种定性分析,不是定量分析。如需要知道蛋白在一个样品中含量高低,可以根据每个蛋白的谱图数量进行粗略估计,谱图数越多,说明该蛋白丰度越高。如要对多个样品的同一个蛋白的含量进行比较,则可选择iTRAQ或者label free法进行相对定量。 Q:胶条鉴定结果中,如何挑选可信蛋白? A:在胶条鉴定中,鉴定蛋白的标准是至少含有一个uniQue peptide,列表中都是鉴定到的蛋白,并给出相应的得分。您可根据得分,结合分子量、等电点等信息筛选目标蛋白。 Q:胶条项目,如何比较几个样品中共有蛋白质和特有的蛋白质? A:可利用文氏图进行分析比对。在地址http://bioinfogp.cnb.csic.es/tools/venny/index.html输入protein ID即可。 Q:胶点鉴定结果与跑出的双向蛋白图谱比较相差较大的情况下,该如何判断一个胶点中给出的几个甚至十几个点蛋白中哪个蛋白可信度最高? A:蛋白质谱鉴定是通过肽段归并到蛋白,因此有些鉴定到的蛋白可能是目标蛋白的同源蛋白或该蛋白的一亚基,而蛋白的人为或天然修饰、降解等情况都会影响该蛋白出现在胶图中的位置。一般来讲,Mascot鉴定得分越高,可信度就越高,其次可以结合分子量、等电点、肽段覆盖率等信息筛选可信度高的蛋白质。 Q:如何保证蛋白的鉴定质量? A:首先,对于肽段和谱图匹配的离子得分(Ion Score),Mascot会给出一个鉴定阈值(Identity Score),如果离子得分(ion score)大于鉴定阈值(identity score),则为可信的肽段匹配;低于阈值的肽段匹配,是不可信的,会被过滤掉。对于不同的离子得分,Mascot会根据候选肽段段的数目和得分来确定这个阈值,所以这个阈值并不是固定的某个值。 为了保证蛋白的可信程度,还可以设置蛋白的特有肽段的个数(UniQue Peptides),即唯一对应某个蛋白的肽段。只有当蛋白含有至少1个uniQue peptide就认为被鉴定到,同时会给出得分。 Q:为什么要进行蛋白质组全谱分析? A:蛋白质组(Proteome)指由一个物种或一个细胞、组织表达的所有蛋白质。蛋白质全谱分析目的在于鉴定样本中尽可能多的肽和蛋白质混合物的组分。基于质谱技术的全谱分析,可为蛋白高通量的定量和修饰分析提供参考信息。 基于高精度液质联用技术进行蛋白质全谱分析,可以对复杂样本进行蛋白种类分析,并进行相应的生物信息分析包括蛋白质的鉴定、GO分类和代谢通路的分析等,为蛋白质组学提供有力工具。 Q:目前可进行蛋白质组全谱分析的物种有哪些? A:只要物种在蛋白质组数据库中存在足够多的数据、基因组已知或 EST(或转录组)数据足够丰富,均可进行蛋白质组全谱分析。对以上条件均不满足的物种,可在进行蛋白质组全谱分析的同时,做一个基因组或转录组测序,以便为蛋白质组全谱分析提供支持。因此,理论上,所有的物种均可进行蛋白质组全谱分析。 Q:全谱分析中不同分析类型的优缺点? 1)SDS‐PAGE‐LC‐MS/MS分析通过电泳技术对样品中的蛋白质进行分离,对分子量在10KDa~100KDa的蛋白质分离效果好、分辨率高。但是,对分子量小于 10KDa 和大于 100KDa的蛋白质、低丰度蛋白、极端酸碱性蛋白、疏水蛋白(如膜蛋白)的分离则存在一些难以克服的困难; 2)HPLC‐LC‐MS/MS分析通过HPLC对样品中的蛋白质进行分离,分离效能高、灵敏度高、应用范围广、分析速度快,此分离方法在对酸碱性、疏水性的蛋白质分离效果优于SDS‐PAGE分离。HPLC的缺点是存在“柱外效应”,被分离物质的任何扩散和滞留都会显著地导致色谱峰的加宽,产生假阳性。 Q:应该如何选择全谱分析方法? A:若待分析对象中包含内在膜蛋白等极性较强的疏水性蛋白质和分子量较大(>100KDa)或较小(<10KDa)的蛋白质时,建议采用 HPLC‐LC‐MS/MS分析法。若待分析对象不以膜蛋白等极性较强的疏水性蛋白质为主且分子量多集中于10~100KDa范围时,建议采用SDS‐PAGE‐LC‐MS/MS分析法。 Q:全谱分析一般能鉴定到多少种蛋白? A:这取决于分析样品的复杂程度、数据库完善度、蛋白含量和蛋白质组分离程度等。如植物来源的样本中蛋白质种类和数量通常比动物来源的样本多,动物组织样本中蛋白质种类和数量比其血液样本多。通常情况下,全谱分析可以鉴定到1000~3000种蛋白。 Q:蛋白鉴定的修饰分析只提供3种特定的分析吗?是否可以鉴定磷酸化、乙酰化等其他修饰?结果中是否可以看到哪一个氨基酸发生了修饰? A: 1)3种常规修饰:氧化,烷基化,乙酰化。 2)一般磷酸化、泛素化前期需要做富集,自然状态下的磷酸化、乙酰化的量非常少,串联质谱根据母离子的丰度选取 topN 进行二级碎裂来检测,若前期不进行富集,最终鉴定到的磷酸化、乙酰化肽段可能不多。 3)多肽信息表中(peptide)包含具体哪一个氨基酸位点发生了修饰。 Q:蛋白制样的过程当中是否加磷酸酶和蛋白酶抑制剂 cocktail? A:需要加,加蛋白酶抑制剂防止蛋白被降解,加磷酸酶抑制剂防止磷酸化的丢失。 Q:CoIP/IP/Pulldown产物跑胶的时候用银染还是考染? A:两种都可以。一般产物比较少,银染灵敏度较高,推荐银染。考染灵敏度低,未出现条带处也可能鉴定到蛋白。
参考文献: [1] Scott DE, Bayly AR, Abell C, Skidmore J. Small molecules, bigtargets: drug discovery faces the protein-protein interaction challenge. NatRev Drug Discov 2016; 15:533-550. [2] Szklarczyk D, Gable AL, Nastou KC, Lyon D, Kirsch R, Pyysalo S,Doncheva NT, Legeay M, Fang T, Bork P, Jensen LJ, von Mering C. The STRINGdatabase in 2021: customizable protein-protein networks, and functionalcharacterization of user-uploaded gene/measurement sets. Nucleic Acids Res.2021 Jan 8;49(D1):D605-D612. doi: 10.1093/nar/gkaa1074. Erratum in: NucleicAcids Res. 2021 Oct 11;49(18):10800. PMID: 33237311; PMCID: PMC7779004. |